Bài 9.7 trang 13 Sách bài tập (SBT) Hóa học 8
Thực nghiệm cho biết nguyên tố natri chiếm 59% về khối lượng trong hợp chất với nguyên tố lưu huỳnh. Viết công thức hoá học và tính phân tử khối của hợp chất. {Hướng dẫn : Để viết đúng công thức hoá học của hợp chất AxBy phải xác định được các chỉ số X, y. Biết rằng, tỉ lệ phần trăm về khối ...
Thực nghiệm cho biết nguyên tố natri chiếm 59% về khối lượng trong hợp chất với nguyên tố lưu huỳnh. Viết công thức hoá học và tính phân tử khối của hợp chất. {Hướng dẫn : Để viết đúng công thức hoá học của hợp chất AxBy phải xác định được các chỉ số X, y. Biết rằng, tỉ lệ phần trăm về khối lượng giữa hai nguyên tố trong hợp chất bằng đúng tỉ lệ khối lượng giữa hai nguyên tố trong 1 phân tử. Từ đây có các tỉ lệ như sau :
- Bài 9.8 trang 13 Sách bài tập (SBT) Hóa học 8
- Bài 10.1 trang 14 Sách bài tập (SBT) Hóa học 8
- Bài 10.2 trang 14 Sách bài tập (SBT) Hóa học 8
- Bài 10.3 trang 14 Sách bài tập (SBT) Hóa học 8
Xem thêm: Bài 9: Công thức hóa học
Thực nghiệm cho biết nguyên tố natri chiếm 59% về khối lượng trong hợp chất với nguyên tố lưu huỳnh.
Viết công thức hoá học và tính phân tử khối của hợp chất.
{Hướng dẫn : Để viết đúng công thức hoá học của hợp chất AxBy phải xác định được các chỉ số X, y. Biết rằng, tỉ lệ phần trăm về khối lượng giữa hai nguyên tố trong hợp chất bằng đúng tỉ lệ khối lượng giữa hai nguyên tố trong 1 phân tử. Từ đây có các tỉ lệ như sau :
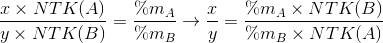
Tính và rút gọn thành tỉ lệ hai số nguyên đơn giản nhất, thông thường thì X, y là hai số nguyên này. Ngoài ra, nếu biết trước phân tử khối của AxBy thì xác định được chắc chắn X và y, không tính dựa theo tỉ lệ như trên).
Trả lời
Gọi công thức của hợp chất là  .Theo đè bài ta có
.Theo đè bài ta có


Công thức hóa học của hợp chất: 
Phân tử khối bằng  (đvC)
(đvC)
